Procédé Haber-Bosch
Synthèse industrielle de l'ammoniac (NH₃) à partir de l'azote atmosphérique et du dihydrogène, sous haute pression et avec catalyseur au fer. Sans lui, on ne nourrirait qu'environ 4 milliards d'humains.
Synthèses de molécules par réactions chimiques contrôlées
Réaction clé
Conditions opératoires
- Température
- 400-450°C
- Pression
- 150-300bar
- Catalyseur
- Fe / Fe₃O₄ promu K₂O + Al₂O₃
- Phase
- gas
Schéma de fonctionnement
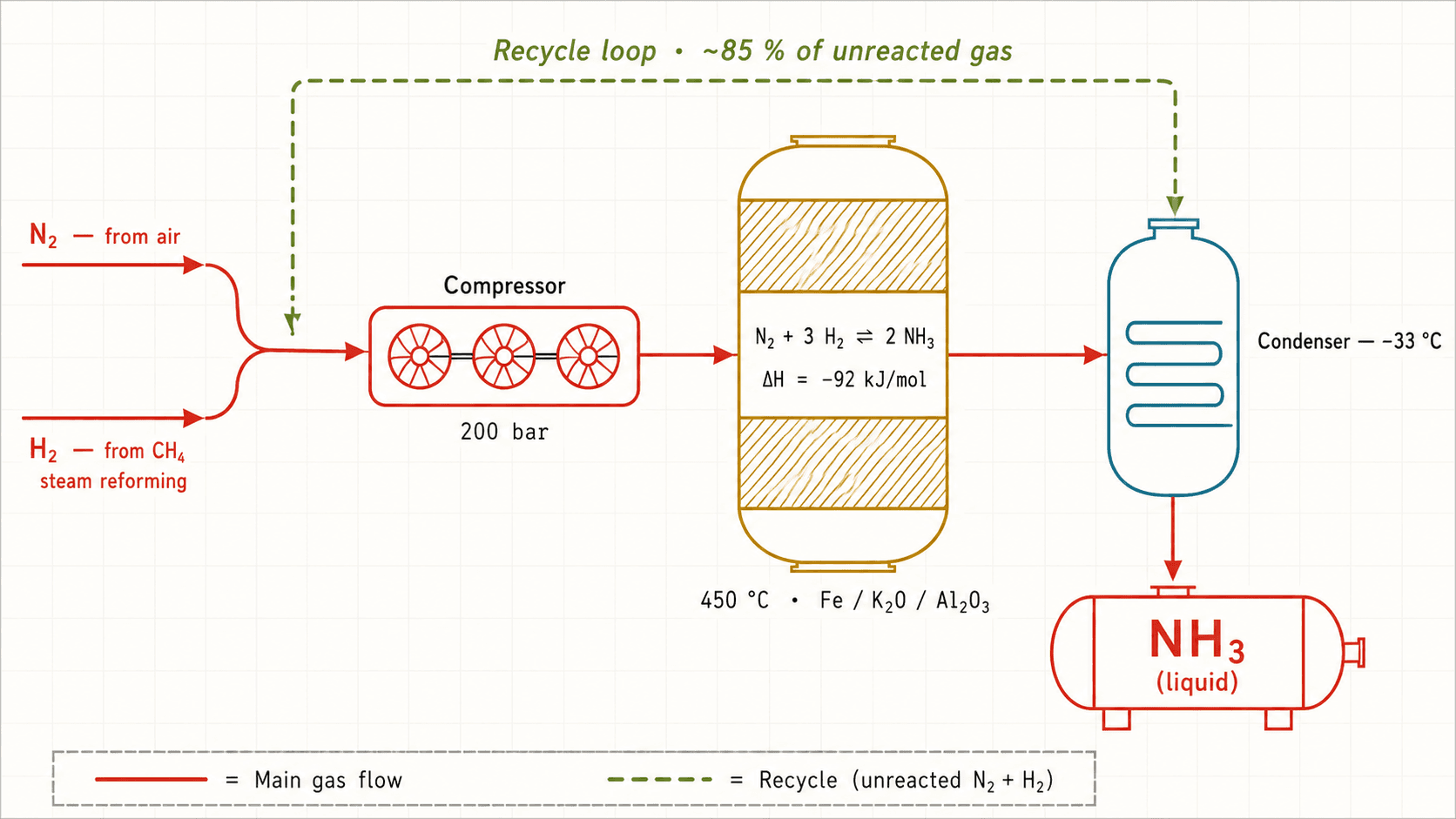
Comment ça marche
Composants clés
Le rôle de chaque pièce maîtresse, et les éléments / composés qu'elle met en jeu.
Compresseur multi-étagé
Comprime le mélange N₂ + H₂ jusqu'à 150-300 bar pour déplacer l'équilibre vers la formation de NH₃.
La compression est réalisée par étages successifs (typiquement 4 à 6) avec refroidissement intermédiaire pour limiter l'élévation de température. Chaque étage augmente la pression d'un facteur ~2-3. C'est l'opération la plus énergivore du procédé : elle représente ~10-15 % de la consommation énergétique totale d'une usine NH₃.
150-300 bar · 4-6 étages · refroidissement inter-étage
Voir aussi :n2h2Réacteur catalytique au fer
Cœur du procédé. Le mélange gaz traverse le lit de catalyseur où ~15 % du N₂ et H₂ se combinent en NH₃.
Le catalyseur est du fer métallique (Fe / Fe₃O₄) finement divisé, promu par K₂O (active la dissociation de N₂) et stabilisé par Al₂O₃ (empêche le frittage à haute température). Le réacteur fonctionne à 400-450 °C — un compromis : plus chaud accélère la cinétique mais déplace l'équilibre vers les réactifs (réaction exothermique). La conversion par passage est limitée à ~15 %, d'où la nécessité de la boucle de recyclage.
400-450 °C · 200 bar · catalyseur Fe / K₂O / Al₂O₃ · ~15 % conv./passage
Voir aussi :n2h2nh3fekalCondenseur réfrigéré
Liquéfie l'ammoniac formé en sortie de réacteur pour le séparer des gaz N₂ et H₂ non réagis.
À 200 bar, NH₃ se condense vers −20 à −30 °C alors que N₂ et H₂ restent gazeux (Tᵉᵇ −196 et −253 °C). Le NH₃ liquide est soutiré par le bas et stocké, les gaz incondensables sont remontés vers le compresseur via la boucle de recyclage. C'est cette séparation simple par changement de phase qui rend le procédé viable.
−20 à −30 °C · 200 bar · NH₃ liquide / N₂-H₂ gazeux
Voir aussi :nh3Boucle de recyclage haute pression
Renvoie au réacteur les ~85 % de gaz non convertis pour atteindre une conversion globale > 97 %.
Sans recyclage, perdre 85 % des réactifs à chaque passage rendrait le procédé non économique. La boucle maintient le mélange sous pression — éviter une décompression suivie d'une recompression économise une énorme quantité d'énergie. Une petite purge évacue les gaz inertes (Ar, CH₄ résiduel) qui s'accumuleraient sinon.
≈ 85 % du débit gazeux · purge inertes ~2 %
Principes physico-chimiques
Les lois fondamentales qui rendent ce procédé possible — et les contraintes qu'elles imposent.
Principe de Le Chatelier (équilibre déplacé par la pression)
La réaction passe de 4 moles de gaz (1 N₂ + 3 H₂) à 2 moles (2 NH₃) — le côté produit a moins de moles. Augmenter la pression force le système à minimiser le volume, donc à former plus de NH₃. C'est exactement pourquoi le procédé travaille à 200 bar : sans ça, l'équilibre est trop défavorable même à haute température.
N₂ + 3 H₂ ⇌ 2 NH₃ (Δn = −2 mol gaz)Catalyse hétérogène (rupture de la triple liaison N≡N)
La triple liaison N≡N (945 kJ/mol) est l'une des plus fortes de la chimie. Sans catalyseur, la dissociation de N₂ exigerait des températures > 1000 °C. Le fer chimisorbe N₂, affaiblit la liaison N≡N et permet à H₂ (lui aussi dissocié à la surface) de s'additionner étape par étape. Le K₂O dope l'activité en cédant des électrons au fer, l'Al₂O₃ structure le support pour empêcher le frittage.
N₂(ads) → 2 N(ads) → … → 2 NH₃S'applique aux composants :reacteur-catalytiqueCompromis cinétique vs. thermodynamique
La synthèse est exothermique (ΔH = −92 kJ/mol). À basse température, l'équilibre favorise NH₃ mais la réaction est trop lente. À haute température, la cinétique est rapide mais l'équilibre se déplace vers les réactifs. 400-450 °C est la plage où la conversion par passage reste correcte (~15 %) tout en maintenant des débits industriels. Toute la conception du procédé tourne autour de ce compromis.
ΔH = −92 kJ/mol · K_eq décroît avec TS'applique aux composants :reacteur-catalytique
Composés impliqués
Réactif
Produit
Production mondiale
Applications principales
- Engrais azotés (urée, nitrates)80 %
- Explosifs et nitrates industriels8 %
- Plastiques (nylon, polyuréthanes)5 %
- Vecteur d'hydrogène (avenir, transport maritime)4 %
- Réfrigération industrielle3 %
Décarbonation et défis actuels
- Ammoniac vert : H₂ produit par électrolyse alimentée 100 % renouvelable (Yara Norvège, NEOM Arabie Saoudite)
- Capture-utilisation du CO₂ co-produit (CCUS, urée bas-carbone)
- Mini-usines décentralisées (~1-10 tNH₃/jour) pour fermes et petites communautés
- Catalyseurs ruthénium-baryum permettant 100 °C et 50 bar — encore en R&D
- Vecteur énergétique : NH₃ comme carburant maritime (IMO 2050) et stockage long terme d'H₂
Procédés similaires ou concurrents
Procédés industriels apparentés — autre voie chimique, autre filière technologique.
- electrosynthese-nh3
Synthèse électrochimique directe de NH₃ à partir de N₂ + H₂O — supprime totalement l'étape Haber-Bosch et la production de H₂. Encore au stade laboratoire, rendements faibles.
- frank-caro
Procédé historique (1898) qui produisait de la cyanamide CaCN₂ comme vecteur d'azote fixé. Abandonné dans les années 1920 face au rendement énergétique très supérieur d'Haber-Bosch.